|
Investigadores de los departamentos de Biología y Biología Molecular de la Universidad Autónoma de Madrid (UAM) han analizado los últimos avances sobre la respuesta de las células de glía tras la isquemia cerebral o ictus, una patología que supone un grave problema de salud pública, siendo la segunda causa de mortalidad y la primera de discapacidad permanente en todo el mundo.
La isquemia es una enfermedad neurodegenerativa provocada por la disminución o bloqueo del flujo sanguíneo cerebral. Actualmente el único tratamiento aprobado consiste en la restauración del flujo sanguíneo al cerebro o reperfusión, que solo es posible durante las primeras horas desde el inicio del ictus, por lo que no todos los pacientes son aptos para esta intervención debido al riesgo de inducir una hemorragia cerebral.
Además, la reperfusión no es totalmente efectiva ya que no reduce la neurodegeneración inducida por la isquemia, lo que provoca pérdida de funciones cerebrales a largo plazo.
En este trabajo de revisión, los investigadores identifican tratamientos farmacológicos con resultados positivos en modelos animales enfocados directamente a las neuronas, pero que aún no han mostrado su efectividad en ensayos clínicos.
Según la opinión de los investigadores, "hay que pasar de un punto de vista neurocéntrico a un abordaje más global que incluya a las células de la glía: microglía, astrocitos y oligodendrocitos".
MICROGLÍA Y ASTROCITOS
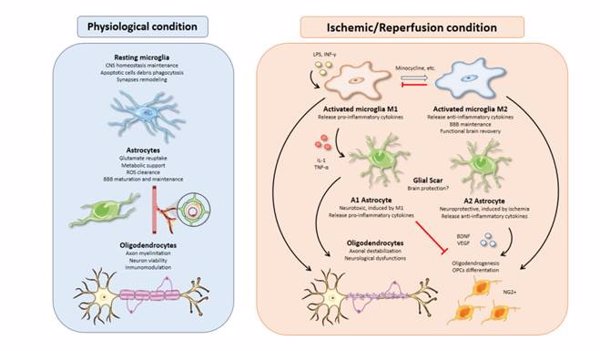
La microglía y los astrocitos participan activamente en los mecanismos patológicos que se desencadenan tras un evento isquémico: inflamación, desestabilización de la barrera hematoencefálica, excitotoxicidad, estrés oxidativo. Pero también intervienen en procesos "beneficiosos", como apoyo metabólico a las neuronas e incluso neurogénesis.
La microglía, considerada como "guardián" del Sistema Nervioso Central (SNC), representa la primera línea de defensa contra el daño isquémico y en consecuencia, son las primeras células que responden tras un ictus.
Los astrocitos, considerados durante mucho tiempo como células con función de soporte neuronal, han mostrado ser imprescindibles tanto en la fisiología del cerebro sano como en la respuesta cerebral al daño. "Los astrocitos se activan tras la isquemia mediante un mecanismo conocido como 'astrogliosis reactiva' que implica su división, profundos cambios morfológicos y una tendencia a concentrarse en la región cerebral que rodea al daño. Parece que esta respuesta tiene como objetivo separar la zona dañada del resto del cerebro 'sano'", apuntan los autores.
Tras la isquemia, la activación tanto de la microglía como de los astrocitos, presenta una dualidad funcional. Por una parte, pueden adquirir una función neurotóxica e inflamatoria (fenotipo M1/A1), y por otra pueden presentar una función neuroprotectora y anti-inflamatoria (fenotipo M2/A2).
"Esto demuestra la necesidad de ahondar en el estudio y conocer qué factores o mecanismos moleculares determinan la aparición de un subtipo celular u otro, ya que el equilibrio entre ambas subpoblaciones determina el grado de severidad de la isquemia. Por otra parte, tratar de potenciar el subtipo 'beneficioso' podría reducir ciertos efectos negativos de la enfermedad", apuntan los autores.
OLIGODENDROCITOS
Los oligodendrocitos son las células responsables de la formación de la vaina de mielina de los axones de las neuronas del SNC. Permiten el aislamiento eléctrico de los axones y determinan la velocidad de conducción del impulso nervioso.
Estas células son altamente sensibles al daño isquémico que provoca su muerte. Esto genera la desestabilización de los axones, lo que afecta a la integridad neuronal, agravando el daño isquémico en el cerebro, con consecuencias negativas en el pronóstico de la enfermedad.
Algunos estudios han demostrado que, a largo plazo, la isquemia cerebral induce una respuesta alternativa en la población de oligodendrocitos, consistente en un incremento de los mismos (oligodendrogénesis) con una tendencia a la colonización de la zona dañada. La función de los nuevos oligodendrocitos generados tras la isquemia todavía es una incógnita, aunque se postula que podrían ser neuroprotectores.
Ante este escenario, los autores consideran relevante investigar en profundidad la respuesta glial a la isquemia cerebral, sobre todo a largo plazo. También destacan la importancia de conocer los mecanismos moleculares implicados en esta respuesta y en determinar claramente la interacción entre las distintas poblaciones de células de glía y entre estas y las neuronas.
"Esto aumentaría las posibilidades de encontrar terapias dirigidas a las células de glía, que podrían ser la clave para reducir el avance de la neurodegeneración desencadenada tras la isquemia cerebral", concluyen los investigadores.
|




