|
El cáncer de vejiga tiene una incidencia anual en España de 22.097 casos, lo que lo convierte en el décimo tumor más frecuente, considerando ambos sexos. Sin embargo, su incidencia es notablemente más elevada en varones, en los cuales ocupa el cuarto lugar en frecuencia, con 18.247 casos nuevos diagnosticados al año, en comparación con los 3.850 en mujeres. En cuanto a la mortalidad, es la sexta causa de muerte por cáncer en varones, con 3.480 fallecimientos al año.
La gran mayoría de los tumores se diagnostican en estadios localizados, donde se pueden ofrecer tratamientos con intención curativa. En los estadios avanzados, los avances acontecidos en los últimos años han logrado mejorar la supervivencia de los pacientes.
Factores de riesgo
La principal causa conocida del cáncer de vejiga es el tabaco, al que se atribuyen más del 40% de todos los casos diagnosticados. El tabaco no sólo afecta nuestra vía respiratoria a través del humo; más de 60 productos carcinógenos contenidos en los cigarrillos son absorbidos y eliminados por la orina, afectando en gran medida a las células de la pared de nuestra vía urinaria.
Algunos estudios defienden la relación entre la infección por HPV (virus del papiloma humano) y el cáncer de vejiga. Se estima que hasta un 17% de estos tumores podrían deberse en parte al hecho de ser portador de serotipos del HPV de alto riesgo.
Existen otros factores de riesgo, como la exposición a algunas sustancias químicas de uso industrial (ciertos metales, tintes y gomas); la exposición a un fármaco llamado ciclofosfamida, que es un tipo de quimioterapia; o la esquistosomiasis, una infección producida por un parásito que suele encontrarse en África y ciertas regiones de América Latina.
Aunque no se ha demostrado de forma clara que la presencia de antecedentes familiares de cáncer de vejiga aumente el riesgo de desarrollar la enfermedad en otros miembros de la misma familia, el diagnóstico en pacientes menores de 60 años debería considerarse con especial atención.
Biología molecular
Los datos del Proyecto Atlas del Genoma del Cáncer (TCGA) han identificado al carcinoma urotelial como uno de los tipos de tumores con mayor nivel de alteraciones genómicas. Se han establecido diferentes clasificaciones, en las cuales los carcinomas uroteliales se han agrupado en diferentes subtipos moleculares. Cada una de ellas se ha desarrollado en poblaciones de pacientes diferentes, empleando diferentes plataformas genómicas. A pesar de las diferencias, cada una identifica fenotipos moleculares que comparten algunas similitudes. Representan una división en tumores basales y luminales, con diferentes subclasificaciones.
Tratamiento
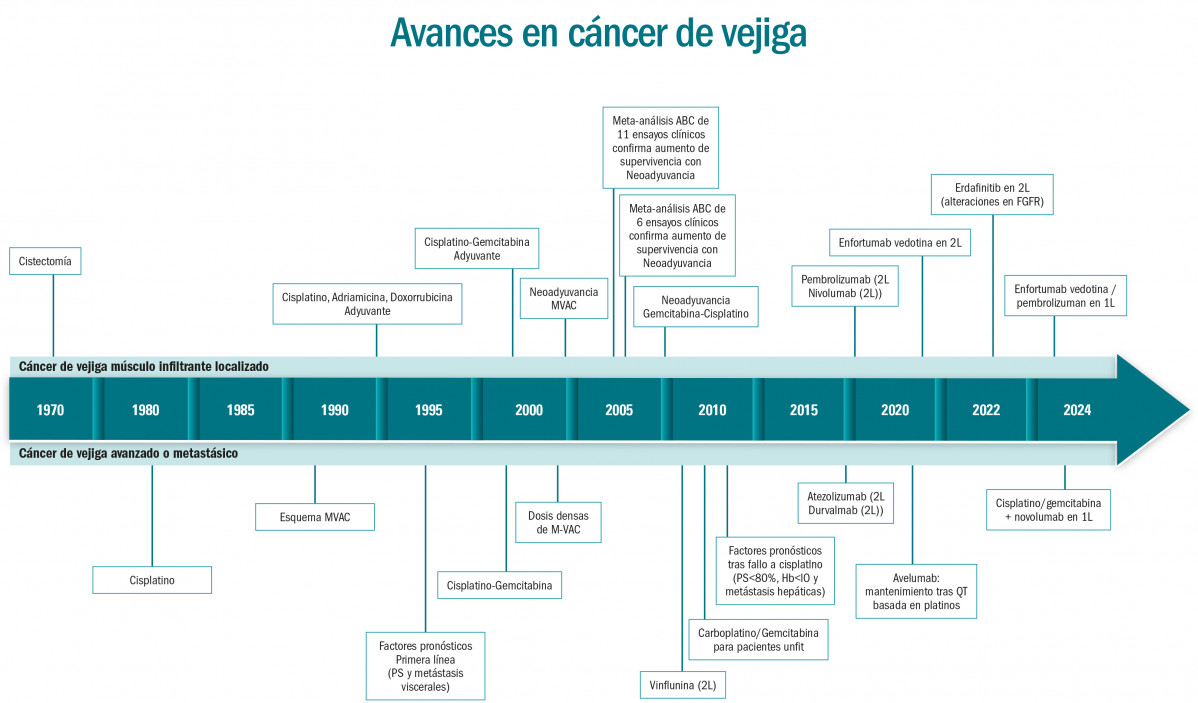
En el carcinoma urotelial músculo-invasivo el tratamiento de elección es la cistectomía radical con linfadenectomía. Se recomienda el tratamiento neoadyuvante con quimioterapia basada en cisplatino para pacientes con tumores cT2/4N0M0, o como tratamiento adyuvante en pacientes con factores de alto riesgo (pT3/4 y/o afectación ganglionar) después de la cistectomía radical. Los regímenes de quimioterapia que pueden emplearse en este escenario son: dosis densas de MVAC (metrotexate, vinblastina, doxorrubicina y cisplatino) o la combinación de cisplatino y gemcitabina.
Además, se puede valorar la preservación de la vejiga empleando lo que se conoce como tratamiento trimodal, que incluye resección transuretral máxima y posterior tratamiento concomitante con quimioterapia y radioterapia, para pacientes seleccionados que deseen evitar o no puedan tolerar la cirugía.
Recientemente, por primera vez, la inmunoterapia ha demostrado su eficacia en el contexto adyuvante. Nivolumab, un anti-PD-1, ha demostrado un impacto positivo en la supervivencia libre de progresión en pacientes con factores de alto riesgo después de la cistectomía radical (pT3/4 y/o afectación ganglionar), que no han recibido tratamiento neoadyuvante, y no son candidatos (o rechazan) el tratamiento con cisplatino. Asimismo, ha demostrado su eficacia en pacientes que tras un tratamiento neoadyuvante presentan factores de alto riesgo (ypT2/4 y/o afectación ganglionar).
Durante los últimos 40 años, el tratamiento de elección para la enfermedad metastásica ha sido la quimioterapia basada en platinos. Sin embargo, en el último año, la inmunoterapia y los anticuerpos conjugados han marcado un hito en el manejo del carcinoma urotelial.
- Entre los años 80 y 90, los esquemas basados en cisplatino (MVAC y gemcitabina/cisplatino) demuestran aumento de supervivencia en comparación con monoterapia y otras combinaciones. Dado que el régimen de gemcitabina/cisplatino tiene un perfil de toxicidad más aceptable, es el tratamiento de elección en primera línea de enfermedad metastásica.
- Sin embargo, entre el 40-50% de los pacientes con enfermedad metastásica no son elegibles para cisplatino (pacientes “unfit”). En estos casos, se puede sustituir por carboplatino.
- En 2020, el tratamiento de mantenimiento con avelumab (anti-PD-L1) en pacientes cuya enfermedad no progresa tras quimioterapia de primera línea basada en platino prolonga la supervivencia global. Esto supone un antes y un después en el tratamiento del carcinoma urotelial avanzado, convirtiéndose en un nuevo estándar de tratamiento.
- De forma más reciente, en el último año, se han presentado dos estudios que han demostrado el beneficio de las combinaciones en primera línea, desbancando por primera vez a los esquemas clásicos con cisplatino en este escenario.
- El estudio ChekMate 901 ha demostrado que la combinación de nivolumab con cisplatino/gemcitabina ofrece beneficio en la supervivencia global frente a la quimioterapia sola.
- Por otra parte, en el estudio EV-302 la combinación de enfortumab vedotina (anticuerpo conjugado frente a nectina-4) y pembrolizumab (anti-PD-1) prolonga la supervivencia global en comparación con un esquema de quimioterapia basada en platino.
En las segundas y sucesivas líneas de tratamiento, en los últimos años, el abanico de opciones también se ha ampliado notablemente.
- La inmunoterapia ha demostrado beneficio en pacientes que progresan a una primera línea de quimioterapia basada en platinos.
- En 2021, el estudio EV-301 demuestra que enfortumab vedotina ofrece beneficio en la supervivencia global en pacientes que progresan a quimioterapia basada en platinos e inmunoterapia.
- El estudio THOR ha demostrado que erdafinitb (inhibidor de FGFR 1-4) aumenta la supervivencia global de pacientes que presentan alteraciones en el factor de crecimiento de fibroblastos (FGFR) tras progresión a platinos e inmunoterapia. Estas alteraciones están presentes en alrededor del 20% de los pacientes.
Todos estos fármacos han podido ver la luz gracias a la realización de ensayos clínicos, y a la generosa participación de los pacientes en ellos. En estos avances, ha habido una participación muy significativa de centros españoles. Seguimos creyendo que la mejor opción, en la medida de lo posible, es la participación en ensayos clínicos. Pero, por encima de todo, es necesario que aquellos progresos que muestren beneficios significativos se incorporen de manera equitativa para todos los pacientes, y que el acceso al mejor tratamiento para su enfermedad sea universal.
Como ya hemos visto, los pequeños avances, tomados de forma conjunta sí son relevantes. De aquí nuestro lema desde la SEOM: En Oncología, cada avance se escribe con mayúsculas. Estos pequeños avances, considerados cada uno de ellos de manera aislada, podrían haber sido considerados de escasa relevancia, pero acumulados entre sí han llevado a cambiar en muchos casos de una manera notable el pronóstico y la calidad de vida de muchos pacientes.
| 



